بیماری پرولاکتینوما
خلاصه مقاله
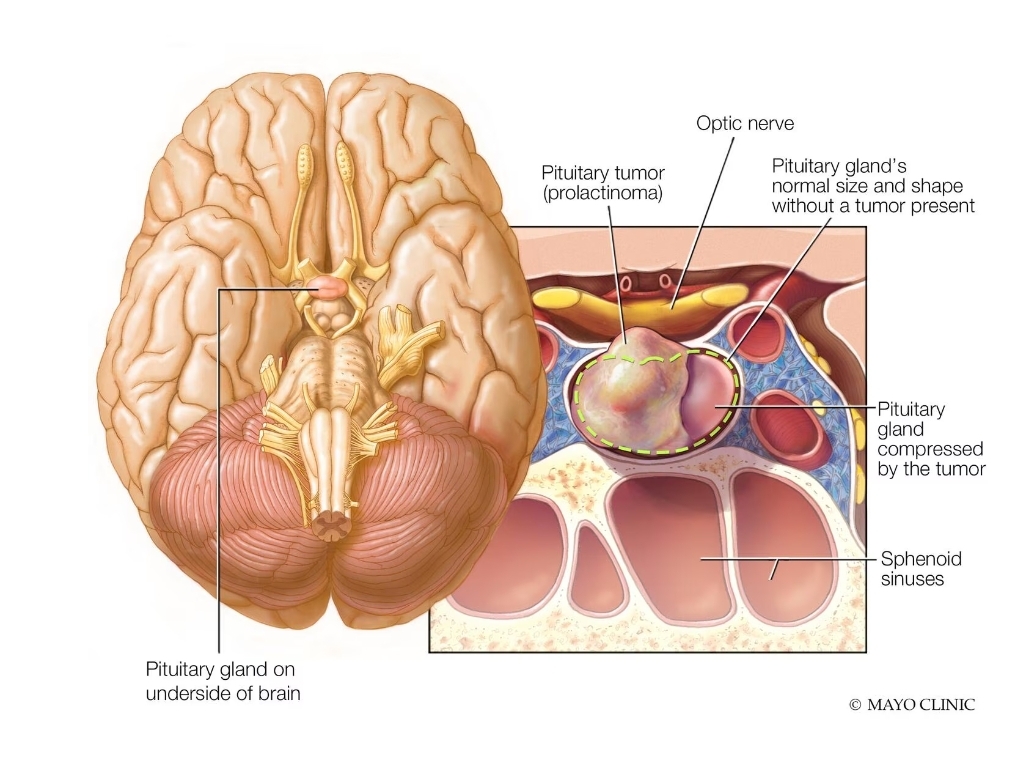
معرفی: پرولاکتینوما شایع ترین شکل تومور نورواندوکرین هیپوفیز (PitNET) است که تقریباً نیمی از این تومورها را تشکیل می دهد. آگونیست های دوپامین (DAs) به طور سنتی درمان اولیه برای اکثر پرولاکتینوم ها بوده و جراحی در مرحله بعدی در نظر گرفته می شود.
#با_مقاله_درس_بخوانیم
#پرولاکتینوما
🔰معرفی: پرولاکتینوما شایع ترین شکل تومور نورواندوکرین هیپوفیز (PitNET) است که تقریباً نیمی از این تومورها را تشکیل می دهد. آگونیست های دوپامین (DAs) به طور سنتی درمان اولیه برای اکثر پرولاکتینوم ها بوده و جراحی در مرحله بعدی در نظر گرفته می شود.
🔰هدف : بررسی مدیریت تاریخی و مدرن پرولاکتینوما از جمله درمان با آگونیست های دوپامین، جراحی ترانس اسفنوئیدال، و درمان چند وجهی برای درمان پرولاکتینومای تهاجمی و تومور نورواندوکرین هیپوفیزهای متاستاتیک، با تاکید بر اثربخشی، ایمنی، و جهت گیری های آینده روش های درمانی فعلی است.
🔰مدیریت: آگونیست های دوپامین از دهه 1970، در ابتدا با بروموکریپتین و اخیراً با کابرگولین، پایه اصلی مدیریت پرولاکتینوما بودند. کابرگولین در 85 درصد بیماران پرولاکتین را عادی می کند و تا 80 درصد باعث کوچک شدن تومور می شود. برداشتن جراحی اولیه میکروپرولاکتینوم ها و ماکروپرولاکتینومای محصور که توسط جراحان مغز و اعصاب هیپوفیز با تجربه انجام می شود، نرخ بهبودی مشابهی با کابرگولین دارند. پرولاکتینومای تهاجمی و تومور نورواندوکرین هیپوفیزهای متاستاتیک باید درمان چندوجهی شامل کابرگولین با دوز بالا، جراحی، پرتودرمانی (ترجیحاً با استفاده از رادیوسرجری استریوتاکتیک در صورت لزوم) و تموزولوماید دریافت کنند. آگونیست های دوپامین یک روش درمانی قابل اعتماد برای اکثر پرولاکتینوم ها باقی می مانند.
🔰تاثیر بر جراحی هیپوفیز آینده: درمان DA، به ویژه بروموکریپتین، ممکن است باعث ایجاد فیبروز در پرولاکتینوما شود. این به عنوان عاملی در عدم بهبودی در برخی از مطالعات جراحی برجسته شده است. این اثر در بیماران تحت درمان با کابرگولین بسیار کمتر است، و مطالعات دیگر تأثیر منفی استفاده از DA قبل از جراحی را بر بهبودی پس از عمل پیدا نکرده اند. با این حال، یک متاآنالیز در سال 2021، تأثیر منفی قابل توجهی از قبل از درمان DA را نشان داد.
🔰رینوره مایع مغزی نخاعی: ماکروپرولاکتینومای بزرگ و تهاجمی می تواند به قاعده جمجمه حمله کند و آن را فرسایش دهد و توده تومور اساساً نقص را مسدود می کند. نشت مایع مغزی نخاعی (CSF) ممکن است با ایجاد رینوره رخ دهد که به نوبه خود منجر به خطر عمده عفونت جدی (مننژیت، آنسفالیت) و پنومونسفالی می شود. بروز رینوره CSF در بیماران ماکروپرولاکتینوما در 7/8 درصد موارد گزارش شده است. در این مطالعه، 30٪ موارد خود به خودی بودند، و 70٪ توسط آگونیست های دوپامین که باعث کاهش اندازه "پلاگ" می شدند، القا شدند. وقوع رینوره CSF مرتبط با DA نیاز به ترمیم جراحی این نقص در تقریباً 90 درصد موارد دار.
🔰نتیجه گیری: پرولاکتینوم ها از نظر بیولوژیکی تومورهای متنوعی هستند که از میکروآدنوم های کوچک غیرفعال تا ماکروآدنوم های بزرگ و مهاجم و در موارد نادر سرطان های متاستاتیک تهاجمی را شامل می شود. آنها حساس ترین تومور نورواندوکرین هیپوفیز برای درمان پزشکی هستند و درمان با آگونیست دوپامین کابرگولین یک روش بسیار مناسب و قابل اعتماد برای اکثر بیماران باقی مانده است. پیشرفتها در جراحی هیپوفیز اکنون به مرحلهای رسیده است که این یک گزینه درمانی خط اول معتبر برای بیماران مبتلا به میکروآدنوم، ماکروآدنومهای غیرتهاجمی و زنانی است که به دنبال بارداری هستند، با این نکته که جراحی توسط جراح مغز و اعصاب هیپوفیز با حجم بالا انجام میشود. جراحی برای افراد مبتلا به مقاومت آگونیست های دوپامین یا عدم تحمل آگونیست های دوپامین مناسب است. درمان چند وجهی برای بیماران مبتلا به پرولاکتینومای تهاجمی و تومور نورواندوکرین هیپوفیزهای متاستاتیک مورد نیاز است، که بر اهمیت مدیریت تومورهای هیپوفیز از طریق یک تیم چند رشته ای تاکید دارد.
📚 منبع
پدیدآورنده: دکتر مهرشاد مهردادیان
✨شکوه دنیای اعصاب در انجمن علمی دانشجویی جراحی اعصاب
با ما همراه باشید.✨
🆔English:@NeurosurgeryAssociation
🆔Persian:@Neurosurgery_Association
مقالات مرتبط
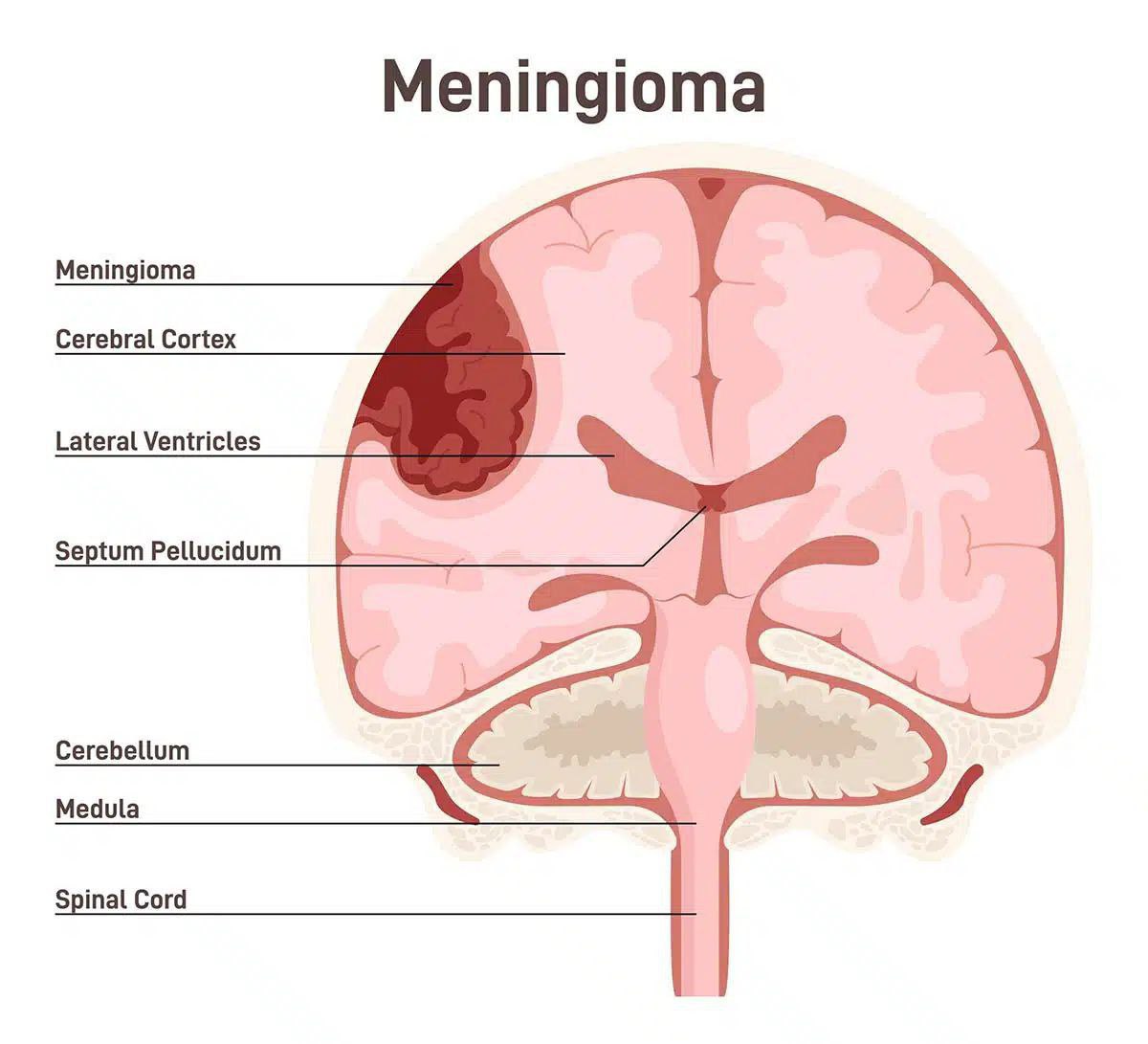
بیماری مننژیوما
مننژیوما یک نوع تومور مغزی است که از بافت های مننژهای مغز (پوششهای مغز) تشکیل شده است. این تومورها معمولاً از بافتهای پوششی مغز (مننژها) شروع میشوند و میتوانند به شکلهای مختلفی در مغز ظاهر گردند.
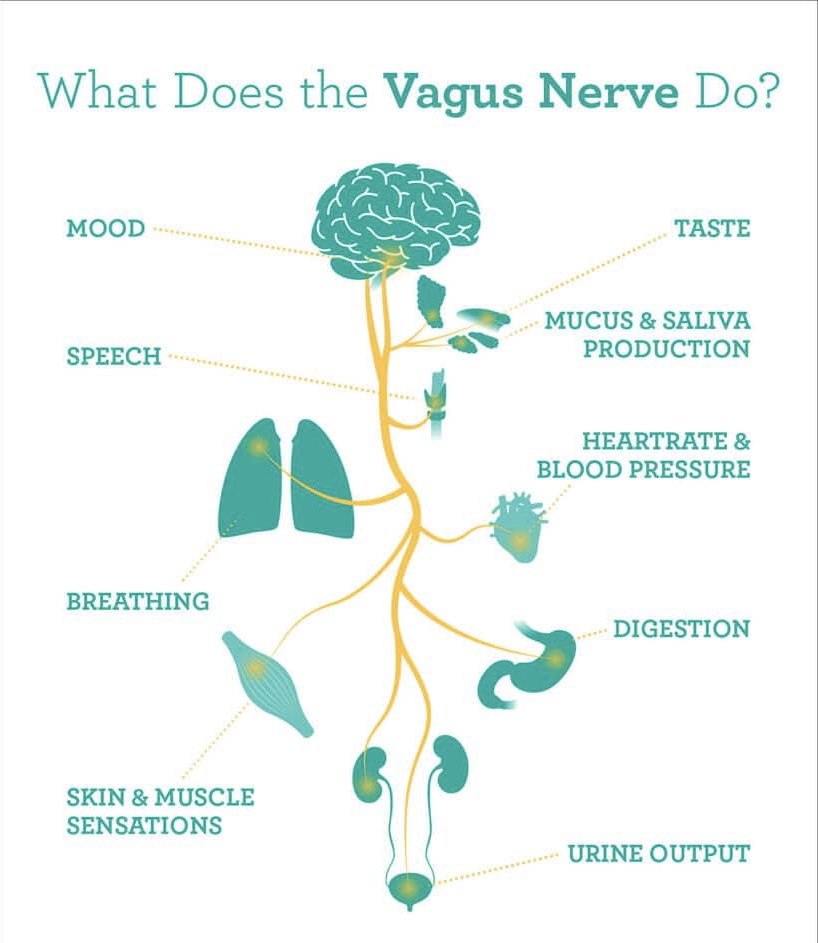
عصب واگ چیست؟ Vagus Nerve
عصب واگ، عصب زوج ۱۰ مغزی است که از ساقه ی مغز، بخش مدولا منشا میگیرد…