درباره ی AVM Arterio Venous Malformation
خلاصه مقاله
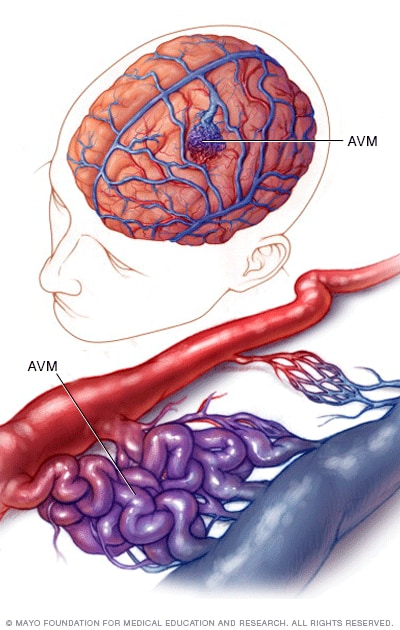
AVM در واقع اشکال در شکل گیری بستر عرپقی در مغز است که شریان ها بدون بستر مویرگی به ورید میریزند و باعث کلافک عروقی میشوند…
#با_مقاله_درس_بخوانیم
#Avm_malformation
✅ تعریف بیماری:
ناهنجاری های شریانی مغزی (Arteriovenous malformation or Avm malformation) از عروق گشاد شده با جریان بالا به نام نیدوس (nidus) تشکیل شده اند که شریانهای تغذیهکننده را با وریدهای تخلیهکننده مستقیماً بدون بسترهای مویرگی به هم متصل میکنند. AVM های مادرزادی با تلانژکتازی خونریزی دهنده ارثی (HHT)، سندرم وایبورن-میسون، بیماری اوسلر-وبر-رندو و سندرم استورج-وبر مرتبط هستند. تغییرات جریان همودینامیک مغزی نقش مهمی در پاتوفیزیولوژی AVM دارد. نیروهای همودینامیک تغییر یافته بین یک شریان و یک ورید می تواند منجر به تشکیل AVM شود که یک ناهنجاری عروقی با جریان بالا است.
✅ علائم بیماری:
حدود 38 تا 71 درصد از بیماران مبتلا به AVM مغزی با خونریزی داخل جمجمه ای مواجه می شوند که بحرانی ترین تظاهرات است. تظاهرات دیگر تشنج (18٪ - 40٪)، سردرد (5٪ - 14٪) و نقص عصبی کانونی (1٪ - 40٪) است. سردرد یکطرفه مکرر ممکن است در 14-5% بیماران وجود داشته باشد. سردرد در AVM های پس سری می تواند میگرن را تقلید کند، زیرا محل پس سری ممکن است با افسردگی گسترده، یک مکانیسم بیماریزای میگرن، مرتبط باشد.
✅ تصویربرداری تشخیصی:
ناهنجاری های مغز را می توان با آنژیوگرافی متعارف متحرک دیجیتال مبتنی بر کاتتر (DSA)، CTA و MRA تشخیص و ارزیابی کرد.
◀️ وضوح مکانی و زمانی DSA منبع شریانی، نیدوس، زهکشی وریدی و عوامل همودینامیک AVMهای مغز را مشخص می کند.
◀️ روش CTA، پس از تزریق داخل وریدی ماده حاجب یددار انجام می شود.
◀️ روشMRA را می توان به صورت 3D TOF MRA، MRA با کنتراست تقویت شده (CE-MRA) یا MRA با استفاده از عوامل مخزن خون انجام داد.
✅ دسته بندی:
بیشترین مورد پذیرش Spetzler-martin بود. این سیستم دسته بندی برپایه سایز (اندازه کمتر از 3 سانت دارای 1 امتیاز، 3 تا 6 سانت دارای 2 امتیاز و بالای 6 سانت دارای 3 امتیاز)، مکان (در مغز فصیح دارای 1 امتیاز، در خارج مغز فصیح دارای 0 امتیاز)، و الگوی خونریزی وریدی (خونریزی وریدی عمقی دارای 1 امتیاز و بدون خونریزی دارای 0 امتیاز) می باشد. این طبقه بندی پنج لایه توسط Spetzler و Ponce با ترکیب AVM های درجه I و II و ترکیب AVM های درجه IV و V به سیستم سه لایه ساده شد زیرا تفاوت در نتایج جراحی بین این جفت های مربوطه کم بود. درمان توصیه شده برای AVM های کلاس A (درجه I و II) جراحی است. درمان چند وجهی برای کلاس B (درجه III) ایده آل است. مشاهده برای کلاس C (درجه IV و V) توصیه می شود. سیستم امتیاز بندی دیگر، سیستم Lawton-Young می باشد. در این سیستم معیارها بر اساس سن (زیر 20 سال دارای 1 امتیاز، بین 20 تا 40 سال دارای 2 امتیاز و بالای 40 سال دارای 3 امتیاز)، خونریزی قبلی (خونریزی داشته دارای 1 امتیاز و بدون خونریزی قبلی بدون امتیاز) و نوع نیدوس (نیدوس منتشر دارای 1 امتیاز و نیدوس فشرده بدون امتیاز) می باشد.
✅ گزینه های درمان
گزینه های مدیریتی شامل مشاهده با مدیریت پزشکی، برداشتن میکروسرجری، آمبولیزاسیون اندوواسکولار و رادیوتراپی استریوتاکتیک است.
◀️ درمان محافظه کارانه ممکن است برای AVM های بدون علامت مغز در نظر گرفته شود. خطر سالانه خونریزی در مطالعات مختلف از 2% تا 4.5% متغیر است. AVM های پاره شده، AVM های زیرین و عمیق و AVM در کودکان و زنان احتمال خونریزی را افزایش داده اند.
◀️ میکروسرجری می تواند درمان آنژیوگرافی AVM و محافظت در برابر پارگی در آینده را به همراه داشته باشد. گرچه میکروسرجری می تواند میزان بالایی از انسداد را ایجاد کند، محدودیت ها شامل محدودیت دسترسی آناتومیک، ادم ناشی از انقباض، پارگی حین عمل، خطر برداشتن بافت طبیعی مغز و ترومبوز عروق تغذیه کننده است. Spetzler-Martin درجه I و II خطر جراحی پایینی دارد و میکروسرجری توصیه می شود. درجه III دارای ریسک متوسط است. درجه IV و V دارای ریسک بالایی هستند. درمان چند وجهی برای درجه III و مشاهده برای گریدهای IV و V توصیه می شود.
◀️ رادیوسرجری جایگزینی برای AVM ها در مکان های گویا و عمیق است که سایر روش ها ایمن نیستند. رادیوسرجری استریوتاکتیک (SRS)، بخش با دوز بالای تابش استریوتاکتیک، باعث از بین رفتن پیشرونده عروق در طی 2 تا 3 سال می شود. با این حال، خونریزی می تواند در این دوره نهفتگی رخ دهد. حذف با یک کسر و دوز حاشیه بالا (18 تا 25 گری)، به ویژه برای ضایعات با حجم کوچک (≤14 سانتی متر مکعب، ≤3 سانتی متر) انجام می شود. AVM های با حجم زیاد (بیش از 10 سانتی متر مکعب) نیاز به رادیوسرجری با مرحله حجمی یا دوز دارند.
ادامه قسمت اول:
◀️در بسیاری از بیماران، جراحی به دلیل موقعیت مکانی یا تخلیه پیچیده وریدی امکان پذیر نیست و به دلیل اندازه بزرگتر از 3 سانتی متر، رادیوسرجری امکان پذیر نیست. آمبولیزاسیون اندوواسکولار یک جایگزین است زیرا احتمال خونریزی در مقایسه با میکروسرجری و رادیوسرجری کمتر است. AVMهای کوچک تک تغذیه کننده و تک محفظه ای که دارای شریان تغذیه مستقیم هستند برای از بین رفتن کامل مطلوب هستند. یکی دیگر از کاربردهای درمان اندوواسکولار کاهش اندازه AVM و حفظ نقاط ضعف کانونی قبل از رادیوتراپی یا جراحی است. انواع آمبولیزاسیون بر اساس اهداف عبارتند از: آمبولیزاسیون قبل از جراحی، قبل از پرتو جراحی، درمان کننده و آمبولیزاسیون تسکین دهنده.
✅روش درمانی ترکیبی
بیش از یک روش برای آن دسته از بیمارانی که AVM در نقاط عمیق دارند و آن دسته از بیمارانی که پس از جراحی AVM باقی مانده دارند، ضروری است. درمان AVM های واقع در گانگلیون های پایه، تالاموس و ساقه مغز به ترکیبی از میکروسرجری، آمبولیزاسیون و رادیوسرجری تبدیل شده است. یکی دیگر از کاربردهای درمان چند وجهی، به حداقل رساندن عوارض در کودکان است.
✅درمان دارویی جدید درحال تحقیق:
استراتژیهای درمانی جدید مبتنی بر پاتوفیزیولوژی AVMs در مرحله آزمایشی هستند. آنها داروهای ضد رگزایی برای کاهش بیان VEGF، داروهای تعدیلکننده ایمنی برای تقویت یکپارچگی عروق و داروهای ضد التهابی برای مهار پروتئازها هستند.
گردآورنده: دکتر لیلا عبدلی
ادیتور: دکتر فرزان فهیم
مقالات مرتبط
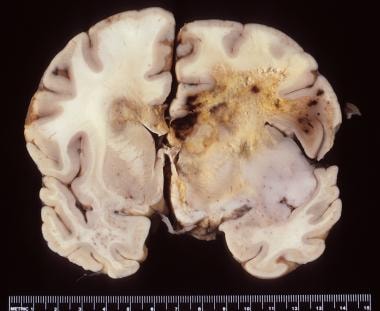
آستروسیتومای منتشر
Diffuse astrocytoma یاآستروسیتومای منتشر یک تومور مغزی با رشد آهسته است که تصور می شود از آستروسیت ها، سلول های حمایت کننده در سیستم عصبی، منشأ می گیرد. بر اساس ویژگی های ژنتیکی طبقه بندی می شود: آستروسیتومای منتشر) IDH-mutant در صورت تشخیص جهش در IDH1 یا IDH2 ) آستروسیتومای منتشرنوع wild( (در صورت عدم شناسایی جهش در IDH ) علائم شامل:سردرد ، تشنج و علائم اضافی به اندازه و محل تومور بستگی دارد. برای تشخیص ازتصویربرداری رزونانس مغناطیسی (MRI) و هیستو پاتولوژیک استفاده می شود. بسته به اندازه و محل تومور، بیماران مبتلا به آستروسیتومای منتشر معمولاً ابتدا با جراحی درمان می شوند. هدف اصلی برداشتن تومور است و از عملکرد حیاتی مغز محافظت میکند – به این کار «حداکثر برداشت ایمن» میگویند. آستروسیتومای منتشر می تواند در نواحی نزدیکی از مغز که حرکات بدن، زبان یا بینایی را کنترل می کند رخ دهد، ممکن است اقدامات ویژه ای برای محافظت از این عملکردها انجام شود. علاوه بر جراحی، بسته به اینکه آیا تومور به عنوان IDH-mutant یا -wildtype طبقه بندی می شود، ممکن است درمان های خاصی مانند شیمی درمانی و پرتو درمانی در نظر گرفته شود.آستروسیتومای منتشر می تواند پس از جراحی عود کند، بنابراین بیماران به طور منظم هم از نظر عود تومور و هم پیشرفت به تومور درجه بالاتر تحت نظر هستند.
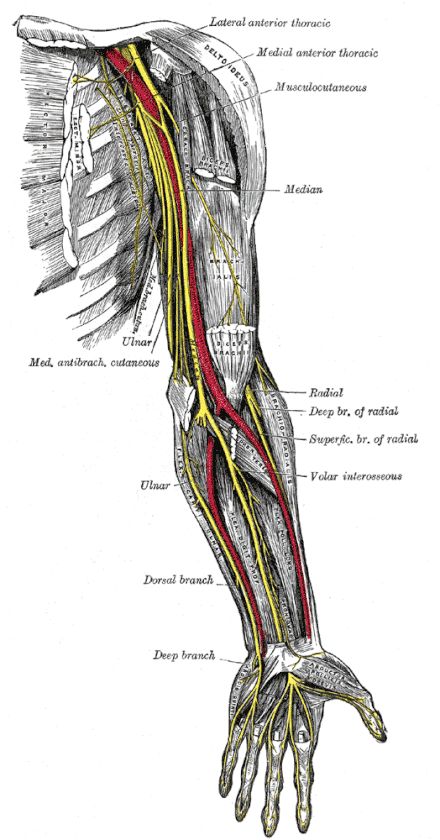
معاینه عصب و اولنار
عصب اولنار امتداد طناب داخلی شبکه بازویی است. این یک عصب مختلط است که عصب را به ماهیچه های ساعد و دست می رساند و در نیمه داخلی انگشت چهارم و کل انگشت پنجم (جنبه اولنار کف دست) و قسمت اولنار قسمت خلفی آن احساس ایجاد می کند. دست (توزیع پوستی اولنار پشتی). گیر افتادن عصب اولنار دومین نوروپاتی گیرافتاده شایع در اندام فوقانی (بعد از گیر افتادن عصب مدین) است. شایع ترین محل گیر افتادن عصب اولنار در ناحیه آرنج یا نزدیک آن است، به خصوص در ناحیه تونل کوبیتال یا در شیار اپی کندیلار (اولنار). دومین مکان محتمل در مچ دست یا نزدیک آن است، همچنین می تواند در ساعد بین این دو ناحیه، زیر مچ (دست) یا بالای آرنج رخ دهد